Keïta, K., Keïta, M., Sogoba, N., Yaro, A.S., Sangaré, D., Keïta, A., Cissé,
B., et Traoré, S.F., 2017. Evaluation de l’impact d’une pulvérisation
intra-domiciliaire en saison sèche sur la transmission du paludisme le long du
fleuve Niger, Mali. Antropo, 38, 87-97. www.didac.ehu.es/antropo
Evaluation
de l’impact d’une pulvérisation intra-domiciliaire en saison sèche sur la
transmission du paludisme le long du fleuve Niger, Mali
Assessing the impact of a dry season indoor residual
spraying on malaria transmission along the River Niger, Mali
Kaly Keïta1,
Moussa Keïta2, Nafomon Sogoba2, Alpha Seydou Yaro2,
Djibril Sangaré2, Abdoulaye Keïta2, Bouréima Cissé2
et Sekou Fantamady Traoré2
1Service de Médecine Interne, CHU du point G, Bamako, Mali.
2Malaria Research and Training Center (MRTC)/ Faculté de Médecine et
d’Odontostomatologie, Bamako, Mali.
Auteur correspondant: Dr Kaly Keita,
Faculté de Médecine et d’Odontostomatologie (FMOS), Université des Sciences,
Techniques et Technologiques de Bamako (USTTB)
Email: keitakaly@gmail.com
Mots
Clés: Saison sèche, nord soudanienne, moustiques, pulvérisation
intra-domiciliaire, cône test.
Keywords: dry
season, northern Sudan, mosquitoes, indoor spraying, cone test.
Résumé
La lutte anti-vectorielle est
essentiellement basée sur l’utilisation des moustiquaires imprégnées
d’insecticide à longue durée (MILD) et la pulvérisation intra-domiciliaire
(PID). Mais le succès de toute méthode de lutte anti-vectorielle et son coût
dépendent de son adaptation aux conditions environnementales locales. Le coût
élevé de la PID peut limiter sa généralisation et sa pérennité d’où la
nécessité de développer de nouvelles approches moins onéreuses adaptées aux
zones d’interventions. C’est dans cet ordre d’idée que le présent travail a été
entrepris dont l’objet est d’évaluer la faisabilité et l’impact possible d’une
PID en saison sèche dans les hameaux riverains du fleuve Niger ainsi que dans
leurs villages-mères sur la transmission du paludisme. Cette étude s’est
déroulée en trois volets: i) la PID, effectuée par des operateurs expérimentés
du 10 au 25 Février 2010; ii) une évaluation de l’efficacité biologique de
l’insecticide utilisé par le cône test de l’OMS 2, 4, 7 et 9 mois après la PID;
iii) un monitorage des paramètres entomologiques de la transmission dans des
hameaux de pêche où eu lieu la PID (tests) et dans d’autres où il n’y a pas eu
de PID (contrôle) ainsi que dans leurs villages mères respectifs (tests vs témoins) de mars à décembre 2010 par
la capture au pyrèthre dans les habitations humaines. Nos résultats ont montré
un taux global de couverture de 88,8%. (978/1101) des cases.
Le taux de
mortalité des moustiques était à 100%
deux mois après la PID période à partir de laquelle l’efficacité
biologique de la lambda-cyhalothrine appliquée
lors de la PID baissait au fil du temps. La
densité était plus faible dans le village test que le village témoin jusqu’au
mois d’août (6 mois après la PID). Le même phénomène était observé dans les
hameaux où les densités étaient plus faibles jusqu’en juin (05 mois après la
PID) dans le hameau test que dans le hameau témoin. Les quatre premiers mois
après la PID, le TIE était plus faible dans le village test que dans le village
témoin, même si la différence n’était
pas significative. La même situation était enregistrée durant les trois
premiers mois dans le hameau test à comparé du hameau témoin. Une seule PID avec la lamdacyhalothrine pendant la
saison sèche le long du fleuve ne protégerait pas la population de la
transmission du paludisme toute l’année, mais réduirait celle-ci de façon
significative au moins trois mois après sa mise en œuvre.
Summary
Vector control is essentially based on the use
of insecticide treated long lasting nets (LLINs) and indoor residual spraying
(IRS). But the success of any vector control method and its cost depend on its
adaptation to local environmental conditions. The high cost of IRS can limit
its extension and sustainability. Therefore, there is a need to develop new and
cheaper approaches tailored to interventions areas. It is in this vein that the
present work was undertaken whose purpose is to assess the feasibility and
possible impact of an IRS during the dry season in fishermen’s hamlets along
the Niger River and in their remote big villages on malaria transmission. This
study was conducted in three parts: i) IRS, performed by experienced operators
from 10 to 25 February 2010 ii) an assessment of the biological effectiveness
of the insecticide using the WHO cone test 2 , 4, 7 and 9 months after IRS iii)
a monitoring of entomological parameters of malaria transmission in hamlets
where an IRS took place (tests) and in others where there was no IRS (control)
and in their respective remotes big villages (test vs control) from March to December 2010 using pyrethrum spray-catch
collection method in human dwellings. Our results showed an overall coverage
rate of 88.8% (978/1101) of the total houses. The mortality rate of mosquitoes
was 100% two months after the IRS, period from which the biological
effectiveness of lambda-cyhalothrin applied during the PID decreased over time.
Density was lower in the test village than in the control village until August
(6 months after IRS). The same phenomenon was observed in hamlets where
densities were lower until June (05 months after IRS) in the test hamlet than
in the control hamlet. The first four months after the IRS, the Entomological inoculation rate was lower in the test
village than in the control village, although the difference was not
significant. The same situation was recorded during the first three months in
the test hamlet comparing to the control hamlet. Therefore we conclude that one
IRS with lamdacyhalothrine during the dry season along the river would not protect the population of
malaria transmission throughout the year, but would significantly reduce it at least three months after the implementation of the
IRS.
Introduction
L’Afrique subsaharienne supporte une part disproportionnée
de la charge mondiale du paludisme. En 2015, 88% des cas de paludisme et 90%
des décès dus à cette maladie sont survenus dans cette région
(OMS, 2016). Au Mali, le paludisme demeure
l’endémie majeure et la première cause de morbidité et de mortalité dans les
groupes les plus vulnérables, à savoir les enfants de moins de cinq ans et les
femmes enceintes. Malgré les progrès accomplis dans le domaine de la prévention
et du traitement, les statistiques sanitaires nationales révèlent que le
paludisme se situe toujours au 1er rang des affections et représente 42% des
motifs de recours aux soins dans les formations sanitaires dans la population
générale (Ministère de la santé du Mali, 2013). Le paludisme est endémique au Mali
avec une intense transmission au cours de la saison pluvieuse dont la durée
varie en fonction des zones éco-climatiques. Subséquemment, nous observons une
extrême variabilité de la situation épidémiologique selon les faciès
éco-climatiques (Doumbo, 1992). En effet, la lutte anti-vectorielle est l’une
des composantes des stratégies globales de lutte antipaludique préconisées par
l’OMS et adopté par la Direction du Programme National de lutte contre le
Paludisme (DPNL) du Mali. Elle est essentiellement basée sur l’utilisation des
moustiquaires imprégnées d’insecticide à longue durée (MILD) et de la
pulvérisation intra-domiciliaire (PID). La PID est une méthode de lutte dont le
principe repose sur le comportement endophile de repos des vecteurs qui
cherchent après chaque repas de sang, des endroits tranquilles et sombres pour
se reposer et digérer ce repas. Cette méthode est appliquée dans quelques
districts sanitaires (Koulikoro et Bla) du Mali depuis 2008 par le DPNLP en
collaboration avec le projet « US President Malaria Initiative ». Il
apparait clairement de ce qui précède que le succès de toute méthode de lutte
anti-vectorielle repose sur la connaissance de la biologie et du comportement
du vecteur incriminé dans la transmission. Pour optimiser ces méthodes, il faut
qu’elles prennent également en compte les conditions environnementales locales
telles que la proximité aux cours d’eaux (Sogoba et al., 2007). Le coût élevé de la PID peut limiter sa
généralisation et sa pérennité d’où la
nécessité de développer de nouvelles approches moins onéreuses adaptées aux
zones d’interventions. La pulvérisation intra-domiciliaire dans les hameaux
réduirait non seulement la densité d’An. gambiae s.l. et la transmission du
paludisme dans ces hameaux, mais aussi dans leurs villages-mères avoisinants. C’est
dans cet ordre d’idée que le présent travail a été entrepris dont l’objet est
d’évaluer l’impact de la PID en saison sèche dans les hameaux riverains du
fleuve Niger ainsi que dans leurs villages-mères avoisinants sur la
transmission du paludisme.
Matériels et Méthodes
Cette
étude s’est déroulée en 3 volets: la Pulvérisation intra-domiciliaire, le test
d’efficacité biologique de l’insecticide, et le monitorage entomologique de la
transmission.
La pulvérisation intra-domiciliaire (PID)
Lieu d’étude: Cette étude s’est déroulée dans huit localités riveraines
de part et d’autre du fleuve Niger situées dans les communes de Bancoumana, du
Mandé, de Sanankoraba, de Dialakoroba, de Niagadina, et de Kourouba. Ces
communes sont situées dans le cercle de Kati, région de Koulikoro, Mali. Ces
hameaux étaient Boumoudjou, Dangassa-somonosso, Terekoudou-somonosso,
Makono-somonosso, Makono-malinké sur la rive droite et Bozokin,
Koursalé-somonosso, Niamanicoro sur la rive gauche (Figure 1).
Période et type d’étude: Il s’agit d’une étude transversale qui s’est déroulée du 10 au 25 février 2010.
Echantillonnage:
Les cases retenues sont celles dont les
propriétaires ont donnée un consentement verbal.
Déroulement:
Après avoir demandé et obtenu le
consentement verbal, des chefs de concessions et des propriétaires de cases,
nous avons procédé à la préparation des cases. Cette opération consistait à
faire sortir tous les aliments et objets encombrants la case afin de faciliter
l’accès aux murs par le pulvérisateur. Ce travail a été fait par les
propriétaires et les guides villageois aidés en cela par les superviseurs et le
coordinateur de l’opération. Les cases une fois préparées, étaient pulvérisées
par les opérateurs. La pulvérisation consistait à asperger sur la façade intérieure
des murs des cases et de la toiture au cas où celle-ci était en chaume ou en
terrasse d’insecticide. Le pourtour extérieur (espace entre le chaume et le
mur) ainsi que la porte d’entrée de la case étaient également traité.
L’insecticide utilisé était de la lambda-cyhalothrine commercialisé sous le nom
d’Icon10CS®. Un sachet (62,5ml) de ce produit était mélangé à un
volume d’eau de 8 litres. Le travail commençait aux environs de 8 heures le
matin et prenait fin vers 11h30. A la fin de la journée de travail l’équipe
amenait le matériel à l’aire de lavage à Bancoumana où l’équipe était basée. La
consigne était donnée aux propriétaires des cases de ne les ouvrir que deux
heures après la pulvérisation, d’attendre environ 30 mn avant de les nettoyer
et de jeter toutes les ordures dans les fosses des toilettes où le cas échéant,
les enterrer.
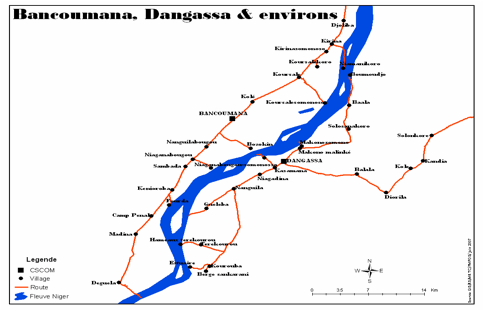
Figure
1.
Carte des villages, et les hameaux ayant bénéficiés la PID.
Figure 1. Map of villages,
and hamlets that benefited from IRS.
Le suivi de l’efficacité biologique
avec les cônes (cône test)
Pour
évaluer la l’efficacité biologique de l’insecticide dans le temps, un hameau où a eu lieu le PID, a été choisi à
chaque rive du fleuve. Il s’agissait notamment du Bozokin sur la rive gauche et
de Dangassa Somonosso sur la rive droite. Dans chacun de ces hameaux 5 cases
ont été choisies aux hasards en tenant compte de la proportion des différents
types de cases (tôle et paille) dans le hameau. Les tests ont été effectués
dans ces cinq cases deux mois (avril), quatre mois (juin) sept mois (septembre)
et neuf mois (novembre) après le PID.
Le kit
pour le bio-essai comprenant: des cônes transparents en plastique, un ruban
adhésif pour fixer les cônes, des tubes d’aspiration courbés et droits, du
papier cartonné, de petits clous, du coton, des gobelets de carton fermés par
un tulle moustiquaire, bracelets, marqueur; cages de moustiques, une caisse en
bois aérée (percée de grands trous), des serpillières.
Des femelles adultes (Colonie d’Anopheles gambiae, souche Kisumu de 2-5 jours d’âge) ont été
élevées au laboratoire du MRTC/FMPOS à Bamako et transportées sur le site
d’étude (village) dans des pots de captures individuels couverts de tulle
moustiquaire. Les pots étaient placés dans des caisses en bois recouvertes de serpillières
légèrement mouillées pour y maintenir une humidité relative élevée. Après un
repos d’une heure au moins et 24 ou 48 heures au plus, ces moustiques étaient
soumis au test.
Ces tests consistaient à: fixer un cône sur le mur
de chacun des quatre cotés de la case traité, garnir le bord du cône de ruban
adhésif, transférer 10 moustiques dans chaque cône et fermer le cône avec un
tampon de coton (utiliser des aspirateurs différents pour les cônes témoins),
après un temps d’exposition de 30 minutes, retirer prudemment les moustiques à
l’aide d’un aspirateur et les transférer dans des gobelets étiquetés, dénombrer
les moustiques assommés (Knock down) ou et morts à la fin de la période
d’exposition. Ne pas éliminer les moustiques assommés car ils peuvent
récupérer, placer un tampon de coton imbibé de solution sucrée sur le tulle de
chaque gobelet, ranger les gobelets dans la caisse aérée et les recouvrir d’un
linge humide, après 24 heures d’observation, dénombrer les moustiques morts et
déterminer le taux de mortalité observée dans les lots tests et les lots
témoins. Le même processus est effectué en fixant un carton sur la surface
traitée et fixer dessus un cône. Ce cône sert comme témoin, si la mortalité
observée chez les témoins est compris entre 5% et 20%, la mortalité dans les
lots tests doit être corrigée en utilisant la formule d’Abott. Si la mortalité
chez les témoins dépasse 20%, l’expérience ne peut être validée.
Monitorage des paramètres
entomologiques de la transmission du paludisme
Pour
le suivi entomologique de la transmission quatre villages (Bancoumana, Dangassa,
Niaganabougou et Kenieroba) et quatre hameaux (Bozokin, Dangassa-somonsso,
Niaganabougou-somonosso et Fourda) ont été choisis. Toutes ces localités sont
situées dans le cercle de Kati (Figure 2).
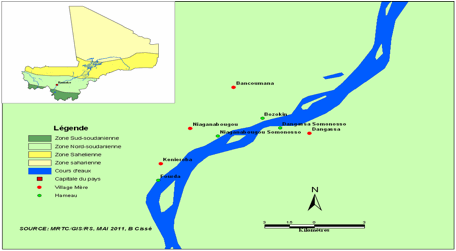
Figure
2. Carte écoclimatique du Mali et
les lieux d’étude pour le monitorage des paramètres entomologiques de la
transmission du paludisme.
Figure 2. Ecoclimatic map of Mali and study sites for the
entomological parameters monitoring of malaria transmission.
Cette étude est de type longitudinal à passages transversaux
d’une durée de quinze jours par mois. Elle a couvert la période de mars 2010 à
décembre 2010. Soixante concessions ont été choisies de façon aléatoire sur la
liste des concessions de chacun des villages. Les 60 cases ont été reparties
selon la proportion des deux types d’habitats (tôle et paille) qui s’y trouve.
Dix cases ont été retenues dans chacun des hameaux à l’exception de Fourda où
douze cases ont été retenues pour les spray-catch.
Deux
séances de capture dans 30 cases ont lieu dans les villages par deux groupes de
captureurs en raison de 15 cases par équipe et 10 cases pour chacun des hameaux
l’exception de Fourda ou 12 cases ont été prospectées. Les captures étaient
faites en pulvérisant dans les chambres un aérosol à base de Pyréthrinoïde (Tétraméthrine
0,15%) et de deux organophosphorés (Dichlorvos 1,20 % et de Fénitrothion 0,40
%) commercialisé sous le label nom de "Premium®".
Avant la pulvérisation de l’insecticide, des draps blancs
étaient étalés sur le plancher de la case pour collectionner les moustiques
moribonds qui y tombent. Tous les spécimens capturés étaient morphologiquement
identifiés, décomptés et classifiés en femelles à jeun, gorgées, semi-gravides
et gravides et conservés case par case dans des tubes contenant du fixateur de
carnoy (3 parties d’éthanol pour 1 partie d’acide acétique glaciale). Une
étiquette portant le numéro de la case et la date de capture accompagne chaque
tube. Le numéro d’identification de la case, le nombre de personnes ayant dormi
dans la case la veille de la capture, le type de case ainsi que le nombre de
spécimens capturés sont enregistrés sur des fiches de base appropriées. Les
moustiques fixés au carnoy sont laissés 48 heures à la température ambiante
avant d’être triés.
Après
dissection sous l’objectif d’une loupe binoculaire, la portion tête-thorax des
moustiques était conservée individuellement dans des tubes Eppendorf de 1,5 ml
vide pour la détermination d’indice d’antigène sporozoïtique (IAS) par la
méthode d’ELISA (Enzyme-Linked ImmunoSorbent Assay) (Beier et al., 1987, 1988).
Recueil
des données pluviométriques
Les
registres de collectes des données pluviométriques de ses différents sites
d’étude ont été utilisés pour la collecte.
Critère
de jugement
Critères de jugement principal
Une baisse significative du taux
d’inoculation entomologique 03 à 06 mois après la PID dans les hameaux tests et
les villages tests comparée aux hameaux témoins et aux villages témoins.
Critères de jugement secondaire
Il s’agit d’avoir un taux de couverture
globale de PID > 80%; un taux d’efficacité biologique à la
Lambda-cyalothrine élevé pendant 03 à 06 mois après la PID; une diminution significative de la densité d’Anopheles gambiae, du taux d’agressivité
d’Anopheles gambiae, du taux
d’infection d’Anopheles gambiae 03 à
06 mois après la PID dans les hameaux tests et les villages tests comparée aux
hameaux témoins et aux villages témoins.
Saisie et
analyse des données
Le logiciel Excel (Microsoft office 2007) a été
utilisé pour la saisie des données et le logiciel SPSS (version SPSS 12.0 for
Windows). L’analyse des donnés ont été faites sur logiciel WinBugs. Ces
comparaisons ont concernée la densité, l’agressivité, le taux d’infection, le
taux d’inoculation entomologique. La densité est calculée en
divisant le nombre d’anophèles capturés par le nombre de cases prospectées. Le
taux d’agressivité (m.a) est égale au nombre total d’anophèles femelles ayant
piquées la veille (gorgée et semi gravide) capturées dans une chambre, divisé
par le nombre de personnes ayant dormi la veille dans la chambre. Le Taux
d’infection correspond au pourcentage d’individus d’anophèles porteurs de
l’indice d’antigène circumsporozoïtique dans la portion tête thorax. Le taux
d’inoculation entomologique (h) représente le nombre de piqûres infectantes
reçues par l’homme et par unité de temps. Les villages tests ont été comparés aux villages
témoins et de même entre hameaux tests et témoins. Les données des villages de
Bancoumana et Dangassa ont été regroupées et forment le village test c'est-à-dire
les villages dont les hameaux ont reçu la PID. Le village témoin était celui
dont le hameau n’a pas été pulvérisé (Kenieroba plus Niaganabougou). Le hameau test (Bozokin
plus Dangassa-Somonosso) était
pulvérisé et le hameau témoin (Fourda plus Niaganabougou-Somonosso) n’avait pas reçu la PID.
Considérations
éthiques
Avant le début de l’étude, l’approbation du comité d’éthique de la Faculté de Médecine, de Pharmacie et d’Odontostomatologie (FMPOS) a été obtenue. Le consentement des populations des sites d’étude a été recherché et obtenu. Les considérations éthiques inhérentes à l’exécution de ce protocole étaient relatives à la PID, au cône test et aux captures de jour par aspersion d’insecticide ou spray-catch. Le consentement éclairé de la population a été cherché et trouvé et aucune case n’a été pulvérisée et de même l’application de cône test sans l’avis de son propriétaire. L’insecticide utilisé était un mélange de Pyréthrinoïde (Tétraméthrine 0,15 %) et de deux organophosphorés (Dichlorvos 1,20 % et de Fénitrothion 0,40 %) commercialisé sous le nom de "Premium®" pour spray-catch et la Lambda-cyhalotrine pour la PID. Ces produits sont reconnus non toxique dans les conditions normales d’utilisation. Les operateurs du PID portaient des combinaisons de protection pour limiter l’exposition à la lambda-cyhalothrine. Les guides villageois travaillant avec l’équipe de recherche avaient des couvre-nez pour éviter les irritations au niveau de la muqueuse nasale que l’aspiration de l’insecticide pourrait provoquer. Les operateurs de la PID et les guides locaux recevaient une rémunération en guise de compensation de leur temps d’activités productrices.
Résultats
|
Localités |
Nombre de cases |
Total |
Taux de couverture |
|
|
Traitées |
Non traitées |
|||
|
Bozokin |
125 |
20 |
145 |
86,2 |
|
Koursalé-somonosso |
28 |
0 |
28 |
100,0 |
|
Niamanicoro |
18 |
0 |
18 |
100,0 |
|
Boumoudjou |
123 |
28 |
151 |
81,5 |
|
Dangassa-somonosso |
134 |
20 |
154 |
87,0 |
|
Terekoudou-somonosso |
12 |
2 |
14 |
85,7 |
|
Makono-Somonosso |
184 |
6 |
190 |
96,8 |
|
Makono-malinké |
354 |
47 |
401 |
88,3 |
|
Total |
978 |
123 |
1101 |
88,8 |
Tableau 1. Taux de couverture de la PID dans huit villages
riverains du fleuve Niger au mois de février 2010.
Table 1. IRS coverage rate
in eight villages along the Niger River in February 2010.
Le taux de couverture moyen de la PID dans les huit
villages était à 88,8%. Le taux de couverture le plus élevé était enregistré à
Koursalé-Somonosso et à Niamanicoro (100%). Il était plus faible à Boumoudjou
(81,5%). La figure 3 indique la variation du taux de mortatlité en fonction du
type de case dans les hameaux tests
après PID.
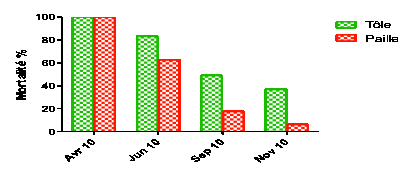
Figure 1. Variation du taux de
mortalité en fonction du type case dans les hameaux tests après PID .
Figure 3. Change in the
mortality rate according to the case type in the test hamlets after IRS.
Le taux de mortalité était à 100% deux mois après la PID
période à partir de laquelle l’efficacité biologique de la lambda-cyhalothrine appliquée lors de la PID
baissait au fil du temps. Elle était plus accentuée dans les cases avec toiture
en paille que les cases avec toiture en Tôle. La
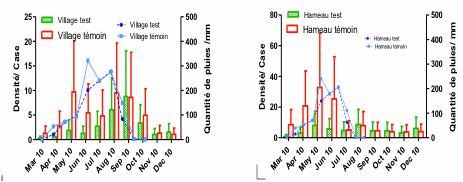
figure 4 montre la variation mensuelle de la densité d’Anopheles gambiae s.l. établie à partir de spray-catch en fonction
de la pluviométrie dans les villages (test et témoin) et hameaux (test et
témoin) de mars 2010 à décembre 2010.
La
densité était plus faible dans le village test que le village témoin jusqu’au
mois d’août (6 mois après la PID). Le même phénomène était observé dans les
hameaux où les densités étaient plus faibles jusqu’en juin (05 mois après la
PID) dans le hameau test que dans le hameau témoin. Parallèlement la densité
augmentait avec la pluviométrie aussi bien dans les villages que dans les
hameaux. Le tableau 2 montre agressivité (nombre de piqûre par homme et par
mois) d’Anopheles gambiae s.l. mesuré
à partir du spray-catch dans les villages test et témoin de mars 2010 à
décembre 2010.
Figure 2.
Variation mensuelle de la densité d’Anopheles
gambiae s.l. établie à partir de spray-catch en fonction de la pluviométrie
dans les villages (test et témoin) et hameaux (test et témoin) de mars 2010 à
décembre 2010
Figure 4. Monthly change in
the density of Anopheles gambiae s.l.
based on spray-catch as a function of rainfall in villages (test and control)
and hamlets (test and control) from March 2010 to December 2010
|
Localités Mois/Année |
Village
test |
Village
témoin |
||||||
|
*ND |
**TAP |
m.a/ mois |
IC à 95% |
*ND |
**TAP |
m.a/mois |
IC à 95% |
|
|
Mars 10 |
333 |
12 |
1,08 |
0,97—1,20 |
419 |
96 |
6,87 |
6,63—7,13 |
|
Avril 10 |
431 |
33 |
2,30 |
2,16—2,44 |
420 |
172 |
12,29 |
11,95—12,92 |
|
Mai 10 |
424 |
128 |
9,06 |
8,77—9,35 |
422 |
632 |
44,93 |
44,29—45,57 |
|
Juin 10 |
447 |
85 |
5,71 |
5,49—5,93 |
411 |
262 |
19,12 |
18,70—19,55 |
|
Juillet 10 |
403 |
219 |
16,30 |
15,91—16,70 |
448 |
357 |
23,91 |
23,46—24,36 |
|
Août 10 |
424 |
407 |
28,80 |
28,29—29,31 |
434 |
573 |
39,61 |
39,02—40,20 |
|
Sept 10 |
409 |
571 |
41,88 |
41,26—42,51 |
438 |
606 |
41,51 |
40,91—42,11 |
|
Oct 10 |
416 |
258 |
18,61 |
18,19—19,02 |
432 |
357 |
24,79 |
24,32—25,26 |
|
Nov 10 |
391 |
79 |
6,06 |
5,82—6,31 |
414 |
89 |
6,45 |
6,21—6,70 |
|
Déc 10 |
416 |
98 |
7,07 |
6,81—7,33 |
408 |
76 |
5,59 |
5,36—5,82 |
Tableau
2.
Agressivité (nombre de piqûre par homme et par mois) d’Anopheles gambiae s.l. mesuré à partir du spray-catch dans les
villages test et témoin de mars 2010 à décembre 2010. ND: Nombre de dormeurs;
TAP: Total ayant piqué la veille.
Table 2. Anopheles gambiae s.l. aggressiveness
(number of bites per man per month) measured from spray-catch in the test and
control villages from March 2010 to December 2010.
Le taux d’agressivité (m.a) par spray catch était plus faible dans le village test que dans le village témoin 07 mois après la PID avec une différence statistiquement significative. On voit qu’il y a au moins 3 fois plus de réduction des agressivités dans le village test comparé au village témoin de mois de mars à juin. Le tableau 3 indique agressivité (nombre de piqûre par homme et par mois) d’Anopheles gambiae s.l. mesuré à partir du spray-catch dans le hameau test et témoin de mars 2010 à décembre 2010.
|
Localités Mois/
Année |
Hameau
test |
Hameau
témoin |
||||||
|
*ND |
**TAP |
m.a/ mois |
IC à 95% |
*ND |
**TAP |
m.a/ mois |
IC à 95% |
|
|
Mars 10 |
75 |
9 |
3,60 |
3,18—4,04 |
84 |
89 |
31,79 |
30,59—33,0 |
|
Avril 10 |
63 |
25 |
11,90 |
11,07—12,77 |
78 |
225 |
86,54 |
84,48—88,62 |
|
Mai 10 |
65 |
83 |
38,31 |
36,82—39,82 |
89 |
327 |
110,20 |
108,00—112,40 |
|
Juin 10 |
64 |
67 |
31,41 |
30,05—32,80 |
87 |
262 |
90,34 |
88,35—92,35 |
|
Juillet 10 |
68 |
67 |
29,56 |
28,28—30,86 |
97 |
53 |
16,39 |
15,60—17,21 |
|
Août 10 |
63 |
85 |
40,48 |
38,92—42,06 |
89 |
101 |
34,04 |
32,84—35,27 |
|
Septembre 10 |
58 |
43 |
22,24 |
21,04—23,47 |
90 |
62 |
20,67 |
19,74—21,62 |
|
Octobre 10 |
62 |
35 |
16,93 |
15,93—17,97 |
82 |
48 |
17,56 |
16,66—18,48 |
|
Novembre 10 |
71 |
28 |
11,83 |
11,04—12,64 |
87 |
46 |
15,86 |
15,04—16,71 |
|
Décembre 10 |
69 |
77 |
33,48 |
32,13—34,85 |
74 |
47 |
19,05 |
18,07—20,06 |
Tableau 3. Agressivité (nombre de piqûre par homme et par mois)
d’Anopheles gambiae s.l. mesuré à
partir du spray-catch dans le hameau test et témoin de mars 2010 à décembre
2010. ND: Nombre de dormeurs; TAP: Total ayant piqué la veille.
Table 3. Aggressiveness
(number of bites per man per month) of Anopheles
gambiae s.l. measured from spray-catch in the test hamlet and control from
March 2010 to December 2010.
Les
quatre premiers mois après la PID, l’agressivité a été réduite au moins de 3
fois dans le hameau test comparé au hameau témoin. Le tableau 4 montre l’indice
d’antigène sporozoïtique (IAS) d’Anopheles
gambiae s.l. établi à partir des échantillons du spray-catch dans les
villages test et témoin de mars 2010 décembre 2010.
|
Localités Mois/ Année |
Village test |
Village témoin |
||||
|
NT |
IAS (%) |
IC à 95% |
NT |
IAS (%) |
IC à 95% |
|
|
Mars 10 |
36 |
2,78 |
0,07—14,53 |
133 |
0,75 |
0,02—4,12 |
|
Avril 10 |
69 |
0,00 |
- |
330 |
0,30 |
0,01—1,68 |
|
Mai 10 |
223 |
1,79 |
0,49—4,53 |
1117 |
0,90 |
0,43—1,64 |
|
Juin 10 |
152 |
0,00 |
- |
670 |
1,94 |
1,04—3,30 |
|
Juillet 10 |
302 |
1,99 |
0,73—4,27 |
578 |
1,38 |
0,60—2,71 |
|
Août 10 |
731 |
1,09 |
0,47—2,14 |
1126 |
0,71 |
0,31—1,40 |
|
Septembre 10 |
1040 |
0,77 |
0,33—1,51 |
1031 |
0,58 |
0,21—1,26 |
|
Octobre 10 |
404 |
6,19 |
4,04—9,00 |
605 |
1,98 |
1,03—3,44 |
|
Novembre 10 |
126 |
6,35 |
2,78—12,13 |
157 |
5,10 |
2,23—9,79 |
|
Décembre 10 |
172 |
6,40 |
3,24—11,15 |
127 |
0,79 |
0,02—4,31 |
Tableau 4. Indice d’antigène sporozoïtique (IAS)
d’Anopheles gambiae s.l. établi à
partir des échantillons du spray-catch dans les villages test et témoin de mars
2010 décembre 2010. NT: nombre testé à l’Elisa.
Table 4. Anopheles gambiae s.l. sporozoite
antigen index based on spray-catch samples in the test and control villages of
March 2010 December 2010.
Le
taux d’infection est resté plus élevé dans le village test que le village
témoin dans la plupart des mois sans que cette différence ne soit statistiquement
significative. Le tableau 5 indique l’indice d’antigène sporozoïtique (IAS) d’Anopheles gambiae s.l. établi à partir
des échantillons du spray-catch dans les hameaux test et témoin de mars 2010
décembre 2010.
|
Localités Mois/ Année |
Hameau test |
Hameau témoin |
||||
|
NT |
IAS (%) |
IC à 95% |
NT |
IAS (%) |
IC à 95% |
|
|
Mars 10 |
15 |
- |
- |
184 |
0,54 |
0,01—2,99 |
|
Avril 10 |
60 |
- |
- |
458 |
0,22 |
0,01—1,21 |
|
Mai 10 |
162 |
- |
- |
722 |
0,69 |
0,23—1,61 |
|
Juin 10 |
114 |
1,75 |
0,21—6,19 |
518 |
0,19 |
0,00—1,07 |
|
Juillet 10 |
94 |
2,13 |
0,26—7,48 |
110 |
0,00 |
- |
|
Août 10 |
161 |
1,24 |
0,15—4,42 |
174 |
0,00 |
- |
|
Septembre 10 |
92 |
1,09 |
0,03—5,91 |
99 |
1,01 |
0,03—5,50 |
|
Octobre 10 |
89 |
3,37 |
0,70—9,54 |
85 |
2,35 |
0,29—8,24 |
|
Novembre 10 |
66 |
1,52 |
0,04—8,16 |
84 |
2,38 |
0,29—8,34 |
|
Décembre 10 |
105 |
- |
- |
88 |
- |
- |
Tableau 5. Indice d’antigène sporozoïtique (IAS)
d’Anopheles gambiae s.l. établi à
partir des échantillons du spray-catch dans les hameaux test et témoin de mars
2010 décembre 2010. NT: nombre testé à l’Elisa.
Table 5. Anopheles gambiae s.l. sporozoite
antigen index based on spray-catch samples in the test and control hamlets of
March 2010 December 2010.
Ce taux d’infection était plus faible trois mois après la PID dans le hameau test que dans le hameau témoin avec une différence significative. Au delà du troisième mois, on observe un taux plus élevé dans le hameau test que le témoin à l’exception de novembre. Tandis qu’il était nul dans les hameaux test et témoin en décembre. La figure 5 montre variations mensuelles du taux d’inoculation entomologique (TIE) d’Anopheles gambiae s.l à après spray-catch dans les villages (test et témoin) et hameaux (test et témoin) de mars 2010 à décembre 2010.
Les quatre premiers mois après la PID, le TIE était plus faible dans le village test que dans le village témoin, même si la différence n’était pas significative. La même situation était enregistrée durant les trois premiers mois dans le hameau test à comparé du hameau témoin.
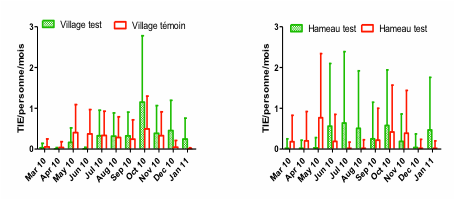
Figure 3.
Variations mensuelles du taux d’inoculation entomologique (TIE) d’Anopheles gambiae s.l à après spray-catch dans les villages (test et témoin)
et hameaux (test et témoin) de mars 2010 à décembre 2010.
Figure 5. Monthly changes
in the rate of entomological inoculation (TIE) of Anopheles gambiae s.l after spray-catch in the villages (test and
control) and hamlets (test and control) from March 2010 to December 2010.
Discussions
Cette étude dont l’objectif était
d’évaluer l’impact possible de la PID en saison sèche dans les hameaux
riverains du fleuve ainsi que dans leurs villages-mères avoisinants sur la
transmission du paludisme. En effet, dans les villages situés à quelque km du
fleuve, les moustiques sont très rares en saison sèche contrairement aux
hameaux où les densités sont relativement
plus élevées (Sogoba et al.,
2007). Une PID bien conduit en saison sèche dans les hameaux pourrait avoir non
seulement un effet sur la transmission du paludisme dans ces hameaux mais aussi
dans les villages environnants où tout au moins retarder la reconstitution de
la population de moustiques pendant la saison des pluies dans ceux-ci. La PID
conduite dans les hameaux a permis d’avoir un taux de couverture moyen de 88,8% ce qui dénote d’une bonne
acceptation par la population locale.
Selon l’OMS pour que la PID ait un impact positif sur la transmission il faut
atteindre un taux de couverture de 80% (OMS, 2016). Les tests d’efficacité
biologique (cône test) effectués deux mois après dans les hameaux tests sur la souche Kisumu sensible ont montré un
taux de mortalité de 100 % 24 heures après l’exposition aux murs traités. Toute
fois la mortalité baissait au fil du temps après la PID (moins de 50% à 7 mois).
Ces résultats diffèrent de ceux observés à Bla et Koulikoro qui avaient trouvé
un taux de mortalité variant entre 79,5 et 89,5% à Koulikoro et 86 à 95 % à Bla
7 mois après la PID (Lambda-cyhalothrine) (Soumaré, 2010). Cette différence
pourrait être due aux conditions climatiques telles que la température, et
l’humidité mais aussi à la nature des matériaux de construction. Par ailleurs
l’efficacité biologique de la Lambda-cyhalothrine variait selon les types de
case. Elle était plus élevée dans les cases en tôle que dans les cases en
paille, respectivement 2, 4,7, et 9 mois après le PID. En effet, une
pulvérisation est efficace pendant 3 à 6 mois en fonction de la formulation de
l’insecticide utilisé et du type de surface pulvérisée. Il apparait évident que
dans cette zone soudanienne, il faut pulvériser plusieurs fois les mêmes
habitations pour protéger la population pendant toute la saison de transmission
du paludisme (OMS, 2016). Le suivi des paramètres
entomologiques de la transmission du paludisme a montré une densité
significativement plus faible dans le hameau test que le hameau témoin jusqu’à
4 mois après la PID. Le même phénomène était observé entre le village test et
le village témoin jusqu’à 6 mois après le PID. Cette différence significative
pourrait être due à la PID effectuée dans les hameaux tests. L’agressivité
moyenne mensuelle était plus faible dans le village test que dans le village
témoin avec une différence statistiquement significative à l’exception des mois
de septembre et novembre. Ces observations pourraient réaffirmer l’impact de la PID sur le village
test. Le taux d’infection était significativement plus faible dans
le hameau test que le hameau témoin trois mois après l’application de
l’insecticide. Par contre, il n’avait pas eu d’impact sur le taux d’infection
dans le village test. Durant les quatre premiers mois
après la PID, le TIE était plus faible dans le village test que dans le village
témoin, même si la différence n’était pas significative et la même situation
était enregistrée durant les trois premiers mois dans le hameau test à comparé
du hameau témoin. Ces observations pourraient
réaffirmer l’impact de la PID sur le hameau test et leurs villages avoisinants.
Conclusion
Le
bon taux de couverture de PID obtenu a permis d’agir sur la densité dans les
hameaux et ou retardé l’apparition de forte densité dans le village test
comparé au village témoin et aussi une réduction du taux d’inoculation entomologique
dans le village test comparé au village témoin trois mois après la PID même si
toute fois la différence n’était pas significative. Une seule PID avec la
lamdacyhalothrine pendant la saison sèche le long du fleuve ne protégerait pas
la population de la transmission du paludisme toute l’année, mais réduirait
celle-ci de façon significative au moins trois mois après sa mise en œuvre, d’où la
nécessité de pulvériser plusieurs fois les mêmes habitations pour protéger la
population pendant toute la saison de transmission du paludisme.
Conflit
d’intérêt: Aucun.
Remerciements. Nous voudrions remercier le PNLP
Mali, les populations des sites d’étude, les guides locaux, le Professeur
Amagana Dolo, le Docteur Ibrahim Baber, le Docteur M’Bouillé Diallo et les
techniciens de laboratoire qui ont contribué à l’atteinte des résultats ici
présentés.
Références
Beier, J.C.,
Perkins, P.V., Wirtz, R.A., Whitmire, R.E., Mugambi, M., Hockmeyer, W.T., 1987,
Field evaluation of an enzyme-Linked immunoSorbent Assay (ELISA) for Plasmodium falciparum sporozoite
detection in anopheline mosquitoes from Kenya. Am J Trop Med Hyg 36 (3), p.459
Beier,J.C.,
Perkings.P.V., Wirts,R.A., Koros,J., Diggs, D., Gargan,T,P.,and Koech, D.K., 1988, Bloodmeal identification by direct
enzyme-Linked immunoSorbent Assay (ELISA),tested on Anopheles
(Diptera:Culicidae) in Kenya. J.Med
Entomol 25 (1), p.9.
Doumbo O., 1992 Epidémiologie du paludisme au
Mali, étude de la chloroquinorésistance et éssai de stratégie de contrôle basée
sur l’utilisation de rideaux imprégnés
de perméthrine associée au traitement systématique des accès fébriles. Thèse de Doctorat en Sciences biologiques, Montpellier
2.
Ministère de la santé du
Mali (2013) Enquête démographique et de santé (EDSM-V) 2012-2013. https://docplayer.fr/10938423-Enquete-demographique-et-de-sante-du-mali-edsm-v-2012-2013.html
OMS, 2016, Paludisme,
aide-mémoire N° 94.
Sogoba,
N., Doumbia, S., Voumatsou,P., Baber, I., Keita,M., Maiga, M., Traore, S. F.,
Toure, A., Dolo, G., Smith, T., Ribeiro, J.M., 2007, Monitoring of larval
habitats and mosquito densites in the Sudan savanna of Mali: implications for
malaria vector control. Am J Trop Med Hyg 77 (1), p.82.
Soumaré H M., 2010, Évaluation
de l’efficacité de la land-cyhalothrine en pulvérisation intra-domiciliaire
dans les cercles de Koulikoro et de Bla au Mali. Thèse de Doctorat en Médecine
(FMPOS).